优化版实验室乙酸乙酯制取装置图及详细步骤
在化学实验室中,制取乙酸乙酯是一项经典的实验,不仅因为其化学过程的趣味性,更因为乙酸乙酯在工业上的广泛应用。本文将详细介绍实验室制取乙酸乙酯的装置图和步骤,并从实验准备、实验步骤、实验现象与产物分析、实验注意事项以及乙酸乙酯的性质和应用等多个维度进行深入探讨。
实验准备
实验药品和仪器
实验所需的药品包括无水乙醇、冰醋酸、浓硫酸和饱和碳酸钠溶液。无水乙醇和冰醋酸作为反应物,浓硫酸则作为催化剂和吸水剂,用于促进反应的进行和减少副产物的生成。饱和碳酸钠溶液用于后续处理,以去除未反应的酸和醇,并收集纯净的乙酸乙酯。

实验所需的仪器包括试管、胶头滴管、控温电加热器、铁架台(带铁夹)、玻璃导管和长导管、量筒(10mL)、水槽、升降台、陶瓷反应板等。这些仪器确保实验过程的顺利进行和产物的有效收集。
实验步骤
步骤一:准备反应混合物
1. 用量筒量取3mL无水乙醇,加入试管中,并将试管置于冰水浴中。冰水浴用于降低温度,减少反应物的挥发。
2. 用量筒量取2mL浓硫酸,在震荡试管的同时,慢慢加入浓硫酸。注意:加入浓硫酸的顺序很关键,必须在乙醇冷却后再加入,以防止乙酸挥发和混合液暴沸。
3. 用量筒量取2mL冰醋酸,加入试管中。待混合物稍冷后,加入几粒沸石(或碎瓷片),以防止反应液暴沸。
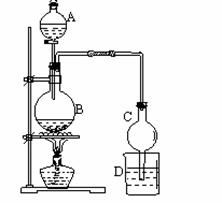
步骤二:设置加热装置
1. 将试管放入盛有热水的烧杯中,用铁夹将其固定在铁架台上。
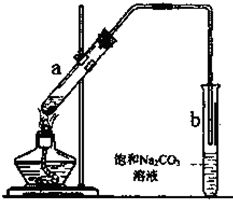
2. 塞上带有导管的橡胶塞,连接装置,确保导管右侧的一端伸入装有饱和Na₂CO₃溶液的试管液面上方2~3cm处。此设计是为了使反应产生的蒸汽通过导管进入饱和Na₂CO₃溶液,从而进行后续处理。
步骤三:加热反应
1. 用控温电加热器给装有热水的烧杯(水浴)加热,控制水浴温度约95℃。注意:温度不能过高,以防止乙醇和乙酸挥发,影响产物纯度。
2. 反应产生的蒸汽经导管进入饱和Na₂CO₃溶液液面上,计时10分钟,观察实验现象。可以观察到饱和Na₂CO₃溶液的液面上有透明的油状液体生成,并可以闻到香味。这是乙酸乙酯的特有性质。
实验现象与产物分析
实验现象
在反应过程中,饱和Na₂CO₃溶液的液面上出现透明的油状液体,并伴随有香味。这是因为浓硫酸、加热的条件下,乙醇和乙酸发生酯化反应,生成无色、透明、不溶于水、有香味的油状液体——乙酸乙酯。
产物分析
乙酸乙酯的化学式为CH₃COOC₂H₅,具有官能团-COOR,是一种酯类化合物。在饱和Na₂CO₃溶液中,乙酸乙酯由于其不溶于水的特性,得以分离和收集。饱和Na₂CO₃溶液的作用包括:降低乙酸乙酯的溶解度,便于收集乙酸乙酯;中和挥发出来的乙酸;溶解吸收挥发出来的乙醇。
实验注意事项
1. 反应混合物用量:本实验中,如果浓硫酸的用量偏多,会导致反应时间过长。可以尝试将浓硫酸体积减小到0.8-1mL,加热时间可缩短到2-3分钟。即乙醇∶浓硫酸∶乙酸体积比为3∶0.8∶2。
2. 烧杯中水的体积:烧杯中加入水的体积不得超过总体积的2/3,但本实验中水可以稍微超过2/3,以尽可能使试管浸在水浴中,减少回流现象,提高产物的蒸出效率。同时,控制温度在95℃,不使水沸腾,降低安全风险。
3. 试剂加入顺序:先加入乙醇,然后在冰水浴中慢慢加入浓硫酸,冷却后再加入冰醋酸。这是为了防止乙酸挥发和混合液暴沸。
4. 导管末端位置:导管末端不能插入饱和Na₂CO₃溶液中,以防止倒吸。
5. 沸石的作用:加入沸石是为了使试管中反应液体均匀受热,防止暴沸。
6. 长导管的作用:长导管不仅用于导气,还用于冷凝回流,防止乙酸和乙醇蒸发损耗。
7. 控温电加热器的作用:控温电加热器用于对反应物加热以提高反应速率
- 上一篇: 王者荣耀星会员激活方法
- 下一篇: 新耳机煲机全攻略
-
 掌握分析天平的正确使用方法资讯攻略12-06
掌握分析天平的正确使用方法资讯攻略12-06 -
 制作纳米胶的详细步骤资讯攻略12-09
制作纳米胶的详细步骤资讯攻略12-09 -
 物理系必看!牛顿环实验揭秘:如何精准测量球面曲率半径?资讯攻略01-14
物理系必看!牛顿环实验揭秘:如何精准测量球面曲率半径?资讯攻略01-14 -
 如何轻松获取QQ飞车点火装置1?资讯攻略11-05
如何轻松获取QQ飞车点火装置1?资讯攻略11-05 -
 饥荒联机版:高效获取懒人法杖的方法资讯攻略01-28
饥荒联机版:高效获取懒人法杖的方法资讯攻略01-28 -
 2013版卡巴斯基安全部队激活码一键使用教程资讯攻略11-18
2013版卡巴斯基安全部队激活码一键使用教程资讯攻略11-18